É uma situação mais frequente nos idosos, imunodeprimidos ou nos doentes sujeitos a procedimentos invasivos.
Título
ABORDAGEM DO DOENTE COM SÉPSIS/CHOQUE SÉPTICO: Criação e Implementação da Via Verde da Sépsis
APPROACH TO THE PATIENT WITH SEPSIS/SEPTIC SHOCK: Design and Implementation of the Sepsis “Green Way”
Nursing nº272
Autor
Dora Maria Ricardo Fonseca Saraiva
Enfermeira Licenciada do Centro Hospitalar Cova da Beira, EPE
RESUMO
O Choque Séptico traduz um processo agudo e disseminado de deficiente perfusão tecidual capaz de provocar distúrbios celulares, metabólicos e hemodinâmicos, pondo em risco a vida do doente. A perfusão dos tecidos torna-se deficiente quando ocorre um desequilíbrio entre o aporte de oxigénio às células e a respectiva necessidade. Este desequilíbrio pode surgir por vários motivos e dele pode resultar disfunção e morte celular.
Os cuidados de enfermagem ao doente em sépsis/ choque séptico são complexos e de grande responsabilidade. Requerem uma profunda compreensão da fisiopatologia da doença e a antecipação dos efeitos de cada intervenção, bem como um conhecimento sólido de todo o processo de actuação.
Este artigo analisa a abordagem do doente com sépsis/choque séptico e expõe a criação e implementação da Via Verde de Sépsis a nível nacional, com vista a uma actualização necessária do suporte teórico e científico da Enfermagem e consequente promoção da qualidade dos cuidados prestados a este tipo de doentes.
Palavras-chave: Sépsis; Choque séptico.
ABSTRACT
The septic shock reflects an acute and widespread process of inadequate tissue perfusion, capable of causing cellular, metabolic and hemodynamic disorders, endangering the patient life. The tissues perfusion becomes deficient when occurs an imbalance between the oxygen supply to cells and their need. This imbalance can happen for several reasons and it can result in dysfunction and cell death.
The nursing care to patients in sepsis / septic shock are complex and of great responsibility. It requires a deep understanding of the disease pathophysiology and the anticipation of the effects of each intervention, as well a solid knowledge of the whole process of action.
This article analyzes the approach of the sick person in these circumstances and exposes the creation and implementation of the Sepsis “Green Way” at a national level, in order to a necessary update of the Nursing theoretical and scientific support and consequent promotion of quality health care provided to such patients.
Keywords: Sepsis; Septic shock.
INTRODUÇÃO
O choque é um estado fisiológico de hipoperfusão tecidular. Independentemente da causa, caracteriza-se por um desequilíbrio entre o transporte e as necessidades de oxigénio e substratos energéticos, o qual pode gerar hipóxia e morte celulares.
A lesão celular induz uma resposta inflamatória que, alterando as características funcionais e estruturais da microcirculação, agrava ainda mais a hipoperfusão. Gera-se assim um ciclo vicioso que, se não for interrompido, pode levar à falência de múltiplos órgãos e, eventualmente, à morte (Smeltezer et al, 2008).
Vários esquemas de classificação de choque têm sido propostos, com o intuito de sistematizar os processos fisiopatológicos subjacentes que, no entanto, se revelam aparentemente diferentes dependendo do tipo de choque instalado.
O presente artigo diz respeito à abordagem específica do doente com choque séptico e traduz um documento actual referente à criação e implementação da Via Verde de Sépsis, determinada através de Circular Normativa da Direcção Geral da Saúde em 2010.
CONCEITOS
Para melhor compreensão do tema e sua problemática importa definir alguns conceitos envolvidos. Assim, de acordo com guidelines internacionais de 2008, distinguem-se três termos:
Sépsis
Infecção suspeita ou documentada associada a um ou mais dos seguintes achados:
- Temperatura > 38° C ou < 36° C
- Frequência cardíaca > 90 batimentos/min
- Frequência respiratória > 20 movimentos/min ou PaCO2 < 32 mmHg
- Leucócitos > 12.000 células/mm3, ou < 4.000 células/mm3 ou > 10% de formas jovens.
Sépsis Grave
- Disfunção orgânica e/ou hipoperfusão tecidual
- Hipoxémia arterial – PaO2/FiO2 < 300
- Oligúria aguda – débito urinário < 0.5 ml/Kg/h por pelo menos 2 horas
- Elevação da creatinina acima de 0.5 mg%
- Anormalidade de coagulação – INR > 1.5 ou aPTT > 60s
- Trombocitopenia < 100.000
- Hiperbilirrubinémia > 4 mg%
- Acidose metabólica
- Hipotensão – definida como pressão arterial sistólica < 90 mmHg ou pressão arterial média < 70 mm Hg ou diminuição na pressão arterial sistólica > 40 mmHg na ausência de outras causas de hipotensão.
Choque Séptico
- Sépsis grave com hipotensão arterial não revertida pela expansão volémica adequada.
Grande parte das sépsis diagnosticadas evoluem para choque séptico e a taxa de mortalidade varia entre 40 a 95% dependendo da demora na identificação e actuação.
Por se tratar da forma mais grave, analisa-se, em seguida, a problemática do choque séptico à luz das orientações nacionais e guidelines internacionais.
ABORDAGEM DO DOENTE COM CHOQUE SÉPTICO
O choque séptico é um tipo de choque distributivo resultante da resposta sistémica a uma infecção grave do organismo. Segundo Thelan et al (2008) este tipo de choque caracteriza-se pela distribuição irregular do sangue nos tecidos dando lugar a áreas hiperperfundidas e outras hipoperfundidas.
O choque séptico, que resulta da resposta do organismo aos microrganismos invasores, é activado pelos sistemas neurológico e endócrino, pelos danos causados aos tecidos e por inúmeros mediadores imunitários. Subsequentemente, sucedem-se disfunções celulares e metabólicas que se repercutem no funcionamento dos órgãos e na perfusão dos tecidos (Smeltezer et al, 2008).
EPIDEMIOLOGIA
Dados portugueses indicam que 22% dos internamentos em unidades de cuidados intensivos são devidos a sépsis adquirida na comunidade. Estes casos originam uma mortalidade hospitalar global de 38%, ou seja, quase três vezes superior à mortalidade dos casos de AVC internados no ano de 2007. A mortalidade das formas mais graves de sépsis, nomeadamente do choque séptico, atinge 51% (Póvoa et al, 2009).
Dados recentes, vindos da Europa e dos Unidos da América (EUA), indicam que a sépsis representa um grave problema de saúde pública, comparável ao acidente vascular cerebral (AVC) e ao enfarte agudo do miocárdio (EAM).
Acresce que a incidência da doença cardiovascular está a diminuir, ao passo que a da sépsis aumenta pelo menos 1,5% ao ano. Este aumento de incidência radica no envelhecimento da população, na maior longevidade de doentes crónicos, na crescente existência de imunossupressão por doença ou por iatrogenia e no maior recurso a técnicas invasivas. A gravidade dos casos de sépsis parece estar também a aumentar, sendo maior o número de doentes com falência orgânica associada à sépsis (sépsis grave). O aumento de incidência determinou aumento do número de mortos por sépsis nos últimos anos, sendo também comparável à mortalidade por AVC e por EAM (DGS, 2010).
ETIOLOGIA
É uma situação mais frequente nos idosos, imunodeprimidos ou nos doentes sujeitos a procedimentos invasivos. As infecções gastrointestinais, urinárias e pulmonares são as mais comuns e a resposta global do organismo bem como o quadro sintomático são independentes do tipo de agente envolvido (Soares et al, 2003).
O choque séptico pode ter origem numa variedade de microrganismos cuja origem pode ser diversa. Capelas (2002) subdivide essa origem em: fontes exógenas (incluem ambiente hospitalar e equipa de saúde) endógenas (incluem a pele do doente, sistema gastrointestinal e geniturinário). Da mesma forma, os factores precipitantes envolvidos são agrupados em factores intrínsecos e extrínsecos conforme esquema 1.
![]()
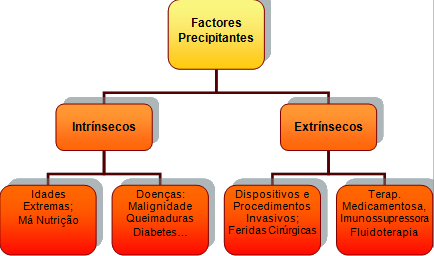
Esquema 1 – Factores precipitantes do choque séptico.
Os principais agentes responsáveis pela génese do Choque Séptico são os bacilos aeróbios gram Negativos, nomeadamente a Escherichia coli com 60% dos casos. Um quarto dos casos resulta da combinação de diversos microrganismos (Capelas, 2002).
FISIOPATOLOGIA
O choque séptico é um estado sistémico que se inicia com a entrada de microrganismos invasores e libertação das respectivas toxinas. Nesta perspectiva, as endotoxinas são libertadas pelas paredes celulares das bactérias gram negativas quando destruídas pelo sistema imunitário humano; e as exotoxinas são libertadas pelas gram positivas e outros microrganismos, enquanto permanecem vivos dentro do organismo.
De forma a dar resposta aos invasores, ocorre uma variedade de mecanismos, entre os quais: activação de mediadores imunitários, lesão do endotélio e activação dos sistemas neurológico e endócrino. Em seguida, ocorrem alterações fisiológicas e patológicas, que inevitavelmente afectam a permeabilidade da membrana capilar, a coagulação, a distribuição do sangue pelos tecidos e o metabolismo.
A resistência vascular sistémica e a tensão arterial baixam. Embora o débito cardíaco aumente, não se pode manter um adequado fornecimento de oxigénio. Daí resulta um fluxo sanguíneo deficiente com hipoxia celular.
Em termos hemodinâmicos, ocorrem dois padrões típicos de alterações no choque séptico: a resposta hiperdinâmica ou precoce e a resposta hipodinâmica ou tardia (Soares et al, 2003). Assim, enquanto um maior metabolismo celular esgota as reservas de glucose e de glicogénio, o choque séptico progride de um estado hiperdinâmico para um estado hipodinâmico (Capelas, 2002), surgindo um desequilíbrio sistémico que consequentemente resulta em hipoxia, lesão, disfunção multiorgânica e morte.
DIAGNÓSTICO
As guidelines internacionais de 2008 recomendam obter culturas apropriadas antes do tratamento antibiótico desde que estas culturas não resultem em atraso na administração do antibiótico.
Para optimizar a identificação do agente causador apontam a realização no mínimo duas hemoculturas antes do início dos antibióticos.
Culturas de outros locais (preferencialmente quantitativa) como urina, liquor, feridas, secreções respiratórias ou outros fluidos corporais que podem ser fonte da infecção devem ser obtidos desde que não resultem em atraso significativo na administração do antibiótico.
AVALIAÇÃO
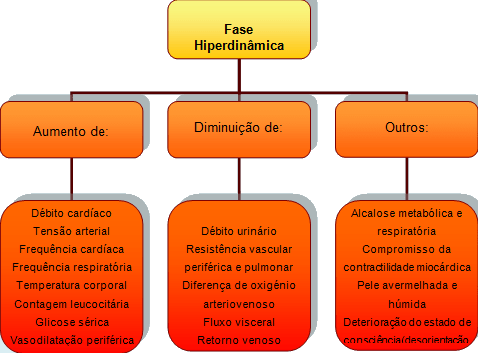
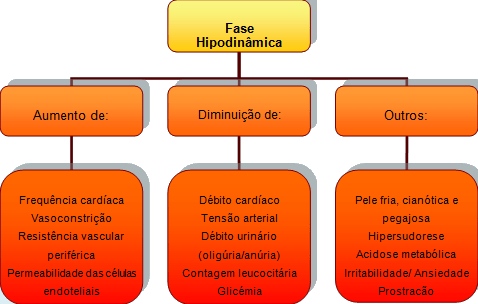
As manifestações clínicas do choque séptico variam consoante o estádio em que o doente se encontra. O estádio inicial do choque é também designado de fase hiperdinâmica ou choque quente (esquema 2), caracterizado por ocorrência de respostas compensadoras. O estádio tardio é designado por fase hipodinâmica ou choque frio (esquema 3), caracterizado pelo desenvolvimento de respostas de descompensação (Thelan et al, 2008). A transição de uma fase para outra pode levar horas ou dias.
![]()
Esquema 2 – Fase hiperdinâmica do choque séptico.
Quando esta combinação de sinais e sintomas está presente, o choque séptico deverá ser considerado, porque o prognóstico é mais favorável do que quando o tratamento é retardado até à fase hipodinâmica.
![]()
Esquema 3 – Fase hipodinâmica do choque séptico.
TRATAMENTO
O tratamento do choque séptico requer uma abordagem multifacetada. Tem como objectivos controlar a infecção, reverter as respostas fisiopatológicas e promover suporte metabólico. Para a consecução destes objectivos torna-se imperativo identificar e tratar a infecção, proporcionar suporte cardiovascular, melhorar a perfusão dos tecidos e iniciar terapêutica nutricional.
As guidelines de 2008 recomendam o disposto no esquema 4.
![]()
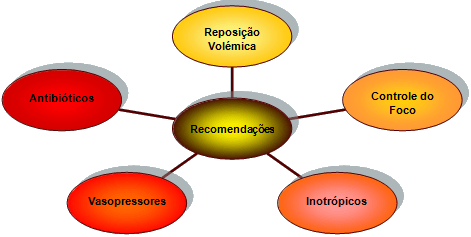
Esquema 4 – Recomendações para o choque séptico.
Analisando cada um per si:
A – Reposição Volémica
1 – Reposição volémica no doente com hipoperfusão tecidual (hipotensão ou acidose láctica) deve ser iniciada logo que a síndrome seja reconhecida e não deve aguardar admissão em unidade de cuidados intensivos.
2 – Em doentes sem hipotensão, uma dosagem sérica elevada de lactato identifica hipoperfusão tecidual.
3 – Prosseguir para atingir os seguintes objectivos durante as primeiras 6 horas de reposição volémica:
- Pressão venosa central > 8 mmHg (12 mmHg para doentes em ventilação mecânica)
- Pressão arterial media > 65 mmHg
- Débito urinário > 0.5 ml/kg/hora
- Saturação venosa central de oxigénio (veia cava) > 70% ou venosa mista (artéria pulmonar) > 65%
Segundo a mesma fonte, o alcance destes objectivos nas primeiras 6 horas reduz a mortalidade em 28 dias.
4 – A expansão volémica com colóides naturais ou sintéticos ou cristalóides, não existindo nenhuma evidência que suporte o uso de um ou outro tipo de solução.
5 – A expansão inicial num ritmo de ≥ 1000 ml de cristalóides ou 300 – 500 ml de colóides em 30 minutos e repetidos na dependência da resposta clínica (alcance dos objectivos) e tolerância (evidencia de sobrecarga volémica).
6 – Diminuir o volume de infusão se ocorrer elevação da PVC sem melhoria hemodinâmica.
7 – Se após a obtenção dos níveis desejados de pressão venosa central a saturação venosa de oxigénio não atingir 70%, as guidelines apontam para considerar infusão de líquidos adicionais e/ou transfusão de hemácias para atingir hematócrito > 30% e/ou dobutamina ate 20 µ g/kh/minuto.
B – Vasopressores
1 – Se a expansão volémica adequada é insuficiente para restaurar a pressão arterial e a perfusão tecidual deve-se iniciar tratamento com vasopressores.
2 – Noradrenalina e dopamina são drogas de primeira escolha para corrigir hipotensão por choque séptico, preferencialmente em cateter central. Sugerimos não utilizar adrenalina ou vasopressina como drogas pressoras iniciais no choque séptico.
3 – Sugere-se adrenalina como droga pressora alternativa de escolha no choque séptico com pouca resposta a noradrenalina ou dopamina.
4 – A monitorização da pressão arterial em doentes com administração de vasopressores deve ser rigorosa e realizada preferencialmente por cateter intra-arterial.
C – Antibióticos
1 – O início de antibióticos intravenosos deve ser o mais precoce possível dentro da primeira hora após reconhecimento da sépsis grave ou choque séptico e após colheita apropriada de culturas.
2 – O esquema empírico inicial deve incluir uma ou mais drogas que sejam activas contra o agente patogénico provável e que tenha penetração no tecido da origem presumida da sépsis. A escolha da droga deve ser baseada no padrão de susceptibilidade dos microrganismos hospitalares e da comunidade.
3 – Sugere-se associação antibiótica quando diagnóstico suspeito ou confirmado de infecção por Pseudomonas como causa do choque, em doentes neutropénicos com sépsis grave.
4 – A associação antibiótica não deve ser utilizada por período > 3 a 5 dias. O escalonamento deve ser realizado logo que possível.
5 – Todos os doentes devem receber dose de ataque plena, com reajuste posterior para funções renal e hepática.
6 – O regime antibiótico deve ser revisto diariamente com base em dados clínicos e microbiológicos para prevenir o aparecimento de resistência, diminuir toxicidade e custos.
7 – Após identificação do patógeno causador, não existem evidências que a associação antibiótica seja mais efectiva que a monoterapia
8 – A duração da antibioterapia deve ser de 7-10 dias. Períodos maiores podem ser apropriados em doentes com resposta clínica lenta, foco infeccioso ao drenado e imunossuprimidos, incluindo neutropénicos.
D – Controle do Foco
1 – Um diagnóstico anatómico específico da infecção considerado como cirúrgico deve ser identificado ou excluído tão rapidamente quanto possível dentro das primeiras 6 horas da apresentação.
2 – Todo o doente com sépsis grave/choque séptico deve ser avaliado quanto à existência de um foco infeccioso corrigível, especificamente pelas seguintes medidas:
- Drenagem de abcessos
- Desbridamento de tecidos necróticos
- Remoção de dispositivos potencialmente contaminados
- Controle definitivo de fonte de contaminação contínua.
E – Inotrópicos
1 – As guidelines recomendam a administração de dobutamina em doentes com disfunção cardíaca caracterizada por altas pressões de enchimento e/ou débito cardíaco baixo;
2 – Na presença de hipotensão deve ser combinada com vasopressores;
3 – Desaconselham o uso de dobutamina em doentes com débito cardíaco normal.
INTERVENÇÕES DE ENFERMAGEM
A identificação dos doentes em risco e a redução da sua exposição aos microrganismos invasores constituem medidas preventivas e são responsabilidade da equipa de enfermagem. Thelan et al (2008) referem procedimentos como a lavagem das mãos e o uso da técnica asséptica como componentes essenciais na prevenção da infecção. Do mesmo modo, devem monitorizar-se sinais de infecção, nos acessos venosos e arteriais, incisões cirúrgicas, feridas traumáticas, cateteres urinários e úlceras de pressão.
Uma vez instalado o choque, as intervenções de enfermagem, dirige-se para a consecução dos objectivos terapêuticos, sendo fundamental a estreita e permanente vigilância hemodinâmica do doente e da perfusão tecidular dos diferentes órgãos. Esta vigilância deverá ser, preferencialmente, efectuada em unidades de cuidados intensivos, dando cumprimento a:
- Vigilância do estado hemodinâmico
- Avaliação da tensão arterial e pressão venosa central
- Avaliação da pressão capilar pulmonar
- Avaliação do gasto cardíaco
- Avaliação da pressão da artéria pulmonar
- Vigilância da perfusão tecidular dos diferentes órgãos: Cérebro (avaliar estado de consciência), Pele (avaliar a coloração, temperatura, sensibilidade e humidade), Rim (avaliação do débito urinário, mediante cateterização vesical (30-50 ml/h)
- Outras avaliações e controles (frequência cardíaca; despiste de arritmias; temperatura corporal; avaliação da função respiração/perfusão; avaliação de parâmetros analíticos, como gasimetria, ionograma sérico e urinário, hematócrito, coagulação, função renal, lactoacidémia; ritmo das perfusões; oxigenoterapia com ou sem suporte ventilatório; balanço hídrico; despiste de dor e analgesia em SOS)
- Proporcionar bem-estar físico e psíquico (posicionamento adequado, higiene adequada)
- O início da reposição nutricional é também de extrema importância pois melhora o estado nutricional do doente, estimula o sistema imunológico e promove a cicatrização
- Apoio psicológico.
CRIAÇÃO E IMPLEMENTAÇÃO DA VIA VERDE DA SÉPSIS
A Direcção-Geral da Saúde (DGS) divulgou uma circular normativa em que determina, por recomendação do Departamento da Qualidade na Saúde, a criação, a nível nacional, da Via Verde da Sépsis (VVS) até ao final de 2011.
Esta decisão surge com base no facto de ser actualmente aceite que uma intervenção precoce e adequada, tanto em termos de antibioterapia como de suporte hemodinâmico, pode melhorar significativamente o prognóstico dos doentes com sépsis grave e choque séptico.
Neste sentido, a DGS considera imperativa a implementação de mecanismos organizacionais que permitam a sua rápida identificação e instituição atempada de terapêutica optimizada.
Sabe-se hoje, por exemplo, que por cada hora que demoremos a administrar antibioterapia apropriada, há uma redução de 7,6% na sobrevivência (Kumar et al, 2006).
Assim, a implementação de um protocolo terapêutico de sépsis permite não só diminuir a mortalidade, mas, também, uma redução substancial dos custos para as instituições.
Neste sentido, a Direcção-Geral da Saúde, no uso das suas competências técnico-normativas, e através da tradução e adaptação das orientações existentes a nível nacional e internacional, validadas por um grupo de peritos, determina, por recomendação do Departamento da Qualidade na Saúde, a criação, a nível nacional, da Via Verde da Sépsis (VVS) (DGS, 2010).
De acordo com a referida circular, da VVS fazem parte todos os Serviços de Urgência (SU) nacionais: SU básicos (SUB), SU médico-cirúrgicos (SUMC) e SU polivalentes (SUP), sendo definidos dois níveis de responsabilidade:
- Nível 1: Serviços de Urgência sem cuidados intensivos (SUB e SUMC de hospitais que não possuam Unidades de Cuidados Intensivos)
- Nível 2: Serviços de Urgência com cuidados intensivos (SUMC que possuam Unidades de Cuidados Intensivos e SUP).
- A existência de uma UCI é determinante, não só para assegurar um local de tratamento e vigilância adequados, mas também porque o passo 4 do algoritmo é altamente dependente do know-how característico da medicina intensiva e do doente crítico, nomeadamente a colocação de cateter venoso central, realização de fluid challenge com avaliação dinâmica da pressão venosa central (PVC), eventual uso de inotrópicos e vasopressores e avaliação de saturação venosa central de oxigénio (SvcO2).
- A implementação da VVS começará pelos Serviços de Urgência de Unidades de Saúde com Cuidados Intensivos (Nível 2), devendo esta primeira fase estar concluída até final de 2010. A concretização da rede deverá estar concluída até final de 2011.
Orientação Organizacional
A. Triagem de Doentes
A identificação e estratificação de doentes devem seguir um processo de três passos.
Passo 1: Identificação de caso-suspeito de sépsis.
O primeiro passoconsiste na avaliação sistemática de todos doentes que recorram ao SU, no momento da triagem geral inicial, nomeadamente da Triagem de Prioridades (Manchester), como possíveis candidatos à VVS. Os critérios VVS não substituem a Triagem de Prioridades (Manchester), antes são aduzidos a esta. A presença de uma suspeita clínica de infecção deve motivar a avaliação obrigatória da frequência cardíaca, frequência respiratória e temperatura corporal (critérios de síndrome de reposta inflamatória sistémica – SIRS). Doentes com uma queixa sugestiva de infecção e pelo menos dois critérios de SIRS (frequência cardíaca superior a 90 bpm, frequência respiratória superior a 20 cpm e temperatura corporal inferior a 36ºC ou superior a 38ºC) avançam para o passo 2.
Passo 2: Confirmação de caso-suspeito de sépsis, de existência de hipoperfusão e de ausência de critérios de exclusão.
O segundo passobaseia-se na rápida reavaliação do doente por um médico do SU, com o objectivo de confirmar suspeita clínica de infecção, avaliar se existe hipoperfusão grave, traduzida por hipotensão (TAS<90mmHg) ou por hiperlactacidemia (>4mmol/l), e se não existem critérios de exclusão da VVS.
Os doentes com confirmação médica da suspeita clínica de infecção e hipoperfusão passam, não havendo critérios de exclusão, para o terceiro passo.
Passo 3: Algoritmo terapêutico
Os dois objectivos fundamentais são a administração de antibioterapia adequada e a optimização da entrega tecidular de oxigénio.
O conceito de antibioterapia adequada radica na utilização de fármacos activos contra o microorganismo causal, em doses maximizadas, com boa penetração no foco de infecção e administrado na primeira hora após o reconhecimento do quadro (Evidência Cientifica de nível 1B). É, portanto, necessária uma clara política de antibióticos no SU que permita que este objectivo seja cumprido.
A prescrição de antibióticos deve seguir as seguintes recomendações internacionais referidas anteriormente.
A terapêutica precoce orientada por objectivos assenta na obtenção, de forma sequencial, de três parâmetros hemodinâmicos claramente definidos, com o intuito de optimizar o aporte de oxigénio aos tecidos periféricos. Estes objectivos são (Evidência Cientifica de nível 1C):
- Pressão venosa central (PVC) > 8 mmHg (ou 12 em doentes ventilados),
- Tensão arterial média (TAM) > 65 mmHg,
- Saturação venosa central de oxigénio (SvcO2) > 70%.
Os objectivos preconizados devem ser atingidos nas primeiras 6 horas após a apresentação, o que implica que os doentes em centros de nível 1, após as medidas iniciais (ie – colheita de exames microbiológicos, primeira administração de antibiótico e início de fluidos), sejam rapidamente transferidos.
CONCLUSÃO
O choque é um estado de grave alteração na perfusão tecidual com indução de disfunções metabólicas importantes em células normais, acarrentando elevado índice de mortalidade se não se agir atempadamente.
Nas últimas décadas tem havido progressos fundamentais no tratamento de doentes em choque e melhorias significativas nos cuidados de enfermagem prestados tanto ao nível da prevenção como do tratamento.
Existe, no caso da sépsis/choque séptico, um conjunto de atitudes que, se realizado numa fase precoce da doença, reduz a morbi-mortalidade. Estas atitudes incluem a identificação e estratificação rápidas de doentes, a utilização de antibioterapia adequada e de estratégias de ressuscitação hemodinâmica guiada por objectivos.
Este artigo analisa a abordagem do doente com sépsis/choque séptico e expõe a criação e implementação de Via Verde de Sépsis a nível nacional, com vista a uma actualização necessária do suporte teórico e científico da Enfermagem e consequente promoção da qualidade dos cuidados prestados a este tipo de doentes.
Bibliografia
Capelas, M. (2002). O choque. Escola Superior de Enfermagem S. Francisco das Misericórdias, Lisboa.
Direcção Geral da Saúde (2010). Criação e Implementação da Via Verde de Sépsis. Circular Normativa. Ministério da Saúde.
Garcia, O.; Doshi, P.; Otero R.; et al. (2008). Early Sepsis management. A meta-analysis of published studies. Ann Emerg Med , 52 (59).
Guidelines Internacionais (2008). Dellinger R., Levy M.; Carlet J.; et. al. Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septic shock. Crit Care Med, 36: 296-327. Acedido em 10/01/2010.
Em: http://www.survivingsepsis.org/system/files/images/2008_Guidelines_Final_.pdf.
Kumar et al. (2006). Duration of Hypotension Before Initiation of Effective Antimicrobial Therapy is the Critical Determinant of Survival in Human Septic Shock. Crit Care Med; 34: 1589-1596.
Póvoa et al. (2009). Influence of vasopressor agent in septic shock mortality. Results from the Portuguese Community-Acquired Sepsis Study. Crit Care Med; 37: 410-416.
Shapiro N.; Howell M.; Talmor D.; et al (2006). Implementation and outcomes of the Multiple Urgent Sepsis Therapies (MUST) protocol. Crit Care Med; 34:1025–1032.
Smeltzer, S. et al (2008). Tratado de Enfermagem Médico-Cirúrgica – Brunner e Suddarth, 11ª Edição, Guanabara Koogan, Rio de Janeiro.
Soares, J. et al (2003). Fisiologia do Choque. Faculdade de Medicina da Universidade do Porto, Porto.
Terzi, R. et al (2005). Estados de choque. In Couto, Renato et al, Emergências Médicas e Terapia Intensiva, Cap. 1, Ratton, Guanabara Kooga, Rio de Janeiro.
Thelan, L.; et al (2008). Enfermagem em Cuidados Intensivos, diagnóstico e intervenção,5.ª edição, Lusodidacta, Lisboa.